欧盟批准Daklinza/Sovaldi联合12周治疗HCV基因型3感染
根据新闻稿显示,Bristol-Myers Squibb公司宣布,欧盟委员会已经批准了治疗慢性丙型肝炎病毒基因型3感染的新方案,即Daklinza与Sovaldi联合使用12周。
更新方案表明Daklinza(达卡他韦,Bristol-Myers Squibb)可以与Sovaldi(索菲布韦,Gilead Sciences)联合使用12周,用于欧盟所有国家无肝硬化患者的治疗,并且不需要联合利巴韦林。根据新闻稿显示,原来治疗基因3型患者,包括那些有或无代偿性肝硬化患者和/或经治患者,需要使用达卡他韦和索菲布韦再加利巴韦林联合治疗24周。
达卡他韦是一种NS5A复合抑制剂,之前被欧洲药品管理局医药产品委员会所看好,基于其与其他HCV药物,包括索菲布韦在内的多个研究的数据所显示。
根据新闻稿显示,2014年8月,欧盟委员会批准Daklinza联合其他医药产品用于基因型1、2、3和4慢性HCV感染的成年患者的治疗。
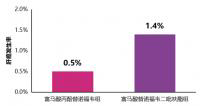
“HCV所产生的负担,尤其是基因型3,在欧洲许多地方仍然很显著,”英国伦敦玛丽皇后大学Blizard研究所肝病学教授Graham R. Foster博士在新闻稿中说。“尽管在治疗中已经有所进步,但使用直接作用抗病毒药物治疗HCV基因型3感染患者仍然是最具挑战性的部分之一。Daklinza联合索菲布韦治疗12周所达到的治愈率表明了,在治疗无肝硬化的基因型3感染患者过程中迈出了积极的一步。”
FDA在7月批准了达卡他韦为治疗HCV基因型3感染患者时经证实其安全性及有效性的第一种药物,并且不需要结合使用干扰素或是利巴韦林。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
热点图文
-
AASLD2018研究进展丨慢乙肝患者治疗期间的肾脏安全管理
在新药取得成功之前,应用口服核苷(酸)类似物(NA)治疗慢性乙型肝炎(简称...[详细]
-
快讯丨TAF治疗4年的肝细胞癌发生率低于TDF
5月17日,在第十届全国疑难及重症肝病大会上,我国香港大学司徒伟基教授交流...[详细]