慢性肾脏病患者,降糖药物怎么选?
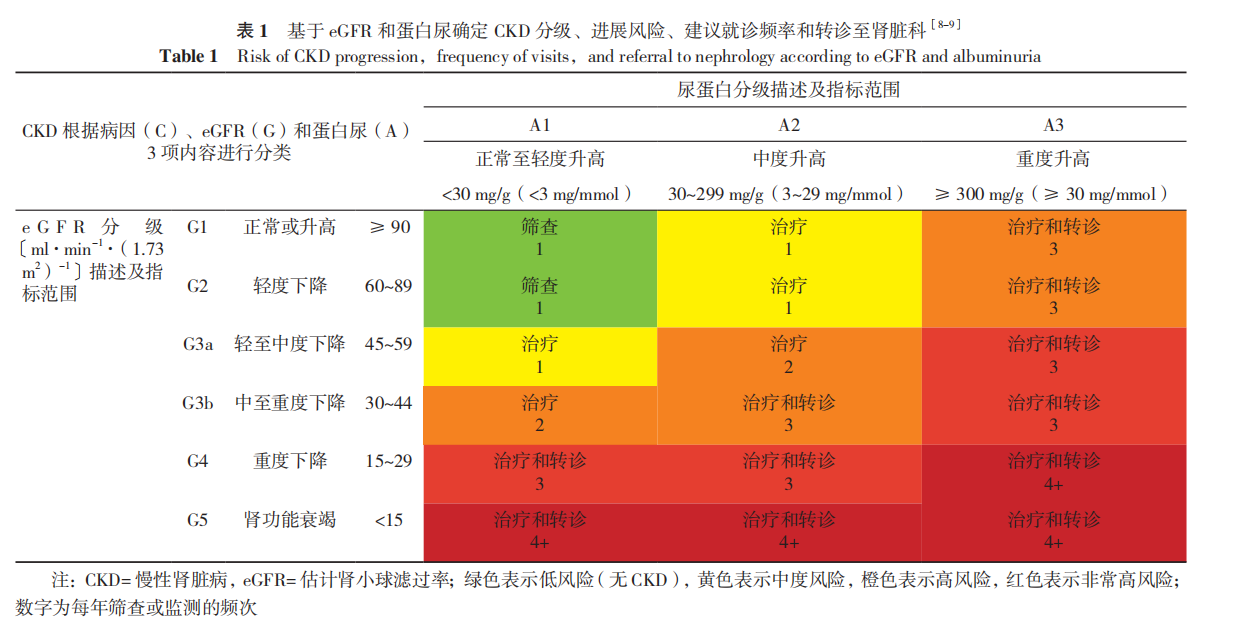
慢性肾脏病(CKD)包括各种原因引起的慢性肾脏结构和功能障碍,定义为各种原因引起的肾脏结构和功能障碍≥3个月,包括肾小球滤过率(GFR)正常和不正常的病理损伤、血液或尿液成分异常,即影像学检查异常;或原因不明的GFR下降(<60ml/min)超过3个月。慢性肾脏病在糖尿病患者中的发病率 >25%,根据慢性肾脏病改善全球预后指南(KDIGO)发布的临床实践指南中,建议联合患者的GFR值及尿白蛋白/肌酐比值(UACR),可以评估患者的CKD分级、尿蛋白分级、疾病进展风险及复查频率,指导患者进行分层治疗(表1)。慢性肾脏病(CKD)和糖尿病患者是肾衰竭、动脉粥样硬化性心血管疾病、心力衰竭和过早死亡的高危人群。糖尿病患者的慢性并发症可累及全身重要器官,其中累及微血管病变可导致糖尿病肾病,导致肾脏微血管障碍和微血管基底膜增厚,引起结节性肾小球硬化、弥漫性肾小球硬化或肾小球渗出性病变,导致肾功能进行性恶化,而大多数降糖药物都是经过肾脏代谢。因此,慢性肾脏病合并糖尿病患者的降糖药物选择是重点也是难点。对于 1型糖尿病患者,胰岛素仍是唯一治疗方法,晚期 CKD 患者需要减少胰岛素剂量;对于2型糖尿病患者,晚期CKD 是低血糖的危险因素,首选不增加低血糖风险的降糖药物。本文主要分析CKD患者口服降糖药的选择。
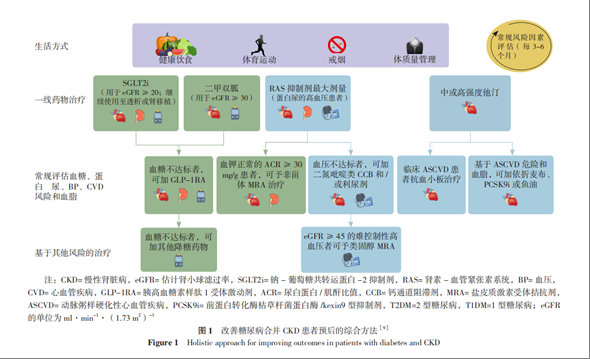
临床常见的降糖药物可分为六大类,分别是磺脲类、格列奈类、双胍类、α-糖苷酶抑制剂、噻唑烷二酮类及新型降糖药(包括钠-葡萄糖协同转运体(SGLT-2)抑制剂、胰高血糖素样肽-1(GLP-1)受体激动剂、二肽基肽酶(DPP-4)抑制剂),对于糖尿病合并CKD患者,一线首选的降糖药物为双胍类及SGLT-2抑制剂,其次为GLP-1受体激动剂(图1),以下详细介绍此3类降糖药物。
① 双胍类: 双胍类主要药理作用是通过抑制肝葡萄糖输出,改善外周组织对胰岛素的敏感性、增加对葡萄糖的摄取和利用而降低血糖。二甲双胍不增加体重,并可改善血脂谱,增加纤溶系统活性、降低血小板聚集性、使动脉平滑肌细胞和成纤维细胞生长受抑制。2022 年《KDIGO 临床实践指南:慢性肾脏病患者的糖尿病管理》提出(表2):二甲双胍推荐用于eGFR ≥ 30ml·min-1·(1.73 m2)-1 的 T2DM 合并 CKD 患者,对于 eGFR 30~44 ml·min-1·(1.73 m2)-1 的患者和 eGFR 45~59 ml·min-1·(1.73 m2)-1 伴乳酸酸中毒风险高的部分患者二甲双胍使用剂量应减少至 1 000 mg/d。二甲双胍在体内以原型随尿排出,肾功能不全时会使其排出减少而增加乳酸酸中毒的风险,故eGFR<30 ml·min-1·(1.73 m2)-1和透析的 T2DM 患者应禁用二甲双胍。
② SGLT-2抑制剂:SGLT2抑制剂可以抑制肾脏对葡萄糖的重吸收,使过量的葡萄糖从尿液中排出,降低血糖。对于 eGFR ≥ 20 ml·min-1·(1.73m2)-1 的 T2DM 合并 CKD 患者,建议使用经证实对肾脏或心血管有益的 SGLT2i;一旦启动,SGLT2i 可以在较低水平的 eGFR 下继续使用。
③ GLP-1受体激动剂:GLP-1以葡萄糖浓度依赖性方式促进胰岛β细胞分泌胰岛素,并减少胰岛α细胞分泌胰高血糖素,从而降低血糖。GLP-1RA 可减少动脉粥样硬化性心血管疾病 (ASCVD )事件和蛋白尿,对于使用二甲双胍和 / 或 SGLT2i 治疗未达到个体化血糖目标或无法服用这些药物的 T2DM 合并 CKD 患者,推荐使用经证实对心血管有益的 GLP-1受体激动剂。
表2:eGFR<45 ml·min-1·(1.73 m2)-1 的降糖药物剂量调整
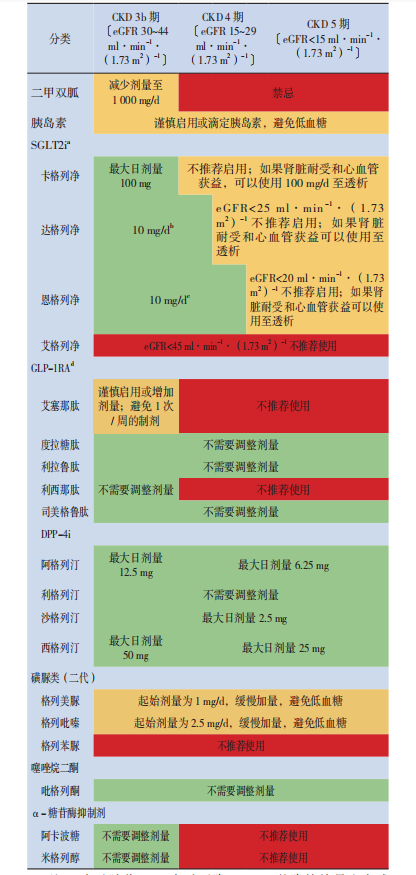
注:a表示随着eGFR 水 平 下 降,SGLT2i 的 降 糖 效 果 也 会 减 弱, 但 对 肾 脏 和 心 血 管 仍 有 益;b表示达格列净在eGFR 25~45 ml·min-1·(1.73 m2 )-1时推荐剂量为10 mg/d;c表示恩格列净作为降糖药物时,在eGFR<30 ml·min-1·(1.73 m2 )-1时不推荐启用,而作为心力衰竭治疗药物时,eGFR<20 ml·min-1·(1.73 m2 )-1时不推荐启用;d表示度拉糖肽、利拉鲁肽和司美格鲁肽证实有显著的心血管保护作用。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理

