小细胞肺癌治疗浅析
众所周知,小细胞肺癌以恶性程度高,容易出现复发转移著称,临床上确诊的患者大都为广泛期,也就相当于是晚期。在最近几年,小细胞肺癌的治疗也有了一些新的进展,比如最近热门的四药联合模式(依托泊苷+卡铂+贝莫苏拜单抗+安罗替尼)获批用于广泛期小细胞肺癌的一线治疗,塔拉妥单抗被FDA批准用于广泛期小细胞肺癌的二线治疗等。这些新的治疗模式或新药的获批毫无疑问给小细胞肺癌的患者带来了更多的治疗选择。由于更新较快,临床应用范围有限。基于此,在下文中,我们将结合最新的循证医学证据以及自身的临床经验对广泛期小细胞肺癌的治疗进行分析,希望能够对大家提供一定的帮助。
一线治疗的选择
PD-1/L1联合EP方案已经成为了广泛期小细胞肺癌一线治疗的选择,代表性的依据就是来自于CASPIN(度伐利尤单抗),IMpower133(阿替利珠单抗),ASTRUM005(斯鲁利单抗)以及CAPSTONE-1(阿得贝利单抗)这4大代表性的临床研究[1]。除此以外,特瑞普利单抗(基于EXTENTORCH研究[2])以及替雷利珠单抗(基于RATIONAL-312研究[3])在广泛期小细胞肺癌的适应症也分别于2024.6.4,2024.6.25获批,这些临床研究的数据在进一步巩固了免疫治疗联合化疗在广泛期小细胞肺癌一线治疗地位的同时,也给临床带来了同类型的药物如何进行选择的问题。
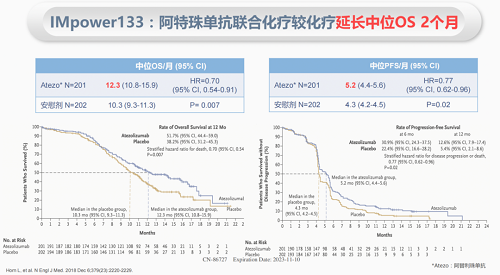
尽管免疫联合化疗已经成为了广泛期小细胞肺癌一线治疗的主要模式,但是在此基础上联合安罗替尼(一种针对VEGF的小分子抑制剂)的横空出世即所谓的四药联合还是打破了三药联合的格局,从某种程度上也可以理解为对原有治疗模式的添砖加瓦。四药联合(也即ETER701研究[4])的数据显示,相比于EP方案而言,四药联合显著提高了一般人群的疗效比如PFS(6.9m vs 4.2m),OS(19.3 vs 11.9m),而且其总体毒副反应大都可耐受。但是,临床在应用的时候,还是要注重治疗人群的选择,毕竟并不是所有的患者都适合四药联合,任何治疗模式都有其优劣势。
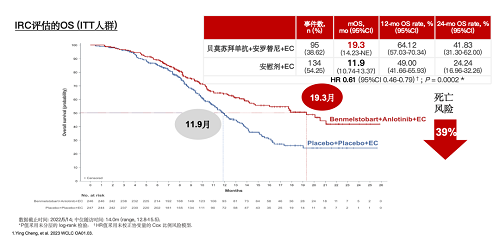
对于四药联合而言,临床应用时还是要注意一些细节,比如患者的体能评分状况良好;要避开相对禁忌人群,比如活动性咯血,肿瘤侵犯大血管,气管等。另外,除了一般人群以外,四药联合尤其适用于特殊人群,比如肝转移,脑转移等,肿瘤负荷比较大需要快速缓解症状的人群(毕竟四药联合相比于单纯化疗而言还是带来了约15%左右的疗效改善,有效率81.3% vs 66.8%)。
最后,多个药物进行联合时还必须重视毒副反应的处理,尤其是毒副反应的鉴别,毕竟不同的毒副反应处理原则就不一样,这一点尤其应该引起临床的重视。
二线治疗的选择
尽管小细胞肺癌一线治疗的有效率高达60-70%,但其疗效难以持久,一般在半年左右就会出现疾病进展,这时候要考虑更换方案,也就是所谓的二线治疗。
按照目前已有的指南与共识来看,小细胞肺癌的二线治疗分为新药与传统意义上的化疗药,新药也就是鲁比卡丁(lurbinectedin,是一种烷基化药物,可结合DNA小沟中的鸟嘌呤残基,形成加合物,并导致DNA螺旋向大沟弯曲)与塔拉妥单抗(Tarlatamab,一款创新型双特异性抗体药物,主要靶向δ样配体3(DLL3)和CD3),传统上的化疗则是紫杉醇,伊利替康,CAV方案(环磷酰胺+阿霉素+长春新碱)等。
不可否认,相比于传统化疗来看,新药的出现还是带来了一定的疗效改善。但是,由于新药的价格昂贵,还没有进入医保而且有些药物比如塔拉妥单抗目前还未在国内获批,所以临床上在新药的使用上还必须考虑治疗的性价比以及药物的可及性等问题。
尽管新药对很多患者而言似乎可望而不可及,但是结合目前已经发表的循证医学证据,将在小细胞肺癌中常用的几类药物比如化疗,抗肿瘤血管形成治疗,免疫治疗等进行合理的排兵布阵,比如将PD-1/L1与抗肿瘤血管药物安罗替尼、阿帕替尼等进行组合 ,还是能够为一部分患者的疗效带来改善,而且还不会出现毒副反应不可控,费用昂贵等情况,至于具体治疗模式的制定,可能更多的是要考验临床医生的经验与水平了。
三线治疗的选择
二线治疗出现疾病进展之后,治疗也就进入了所谓的三线模式。在三线治疗上,可供选择的药物或者方案很少。基于ALTER1202的研究[5]结果,2019年NMPA批准了安罗替尼用于广泛期小细胞肺癌三线治疗的适应症,这也是目前国内外唯一获批的用于广泛期小细胞肺癌的抗肿瘤血管形成小分子抑制剂,除了针对一般人群以外,从亚组分析来看,安罗替尼能够改善既往接受胸部放疗患者、存在胸膜转移和肝转移等患者的生存获益。结合最近刚获批的四药联合用于一线治疗的证据,安罗替尼也几乎实现了在广泛期小细胞肺癌治疗中的全线贯通,可以联合应用也可以单用,可以一线使用,也可以后线使用。对于后线使用,尤其适用于一部分体能状况差,无法耐受化疗或者拒绝化疗的小细胞肺癌患者。
结语
综上所述,小细胞肺癌的治疗虽然总体上看似平淡无奇,波澜不惊,但是还是在不择不饶的向前进步。虽然目前存在的问题还有很多,而且新药在一定程度上带来疗效改善的同时也会带来新的问题,比如双抗特有毒副反应的处理(CRS也即细胞因子释放综合症,ICANS也即免疫效应细胞相关神经毒性综合症等),目前已有治疗模式的优选等。但是我们还是可以清晰的看到在肿瘤治疗模式总体向前推进以及个体化治疗模式的加持下,小细胞肺癌的现状还是非常有希望在不久的将来出现大的改变,从而为更多的患者带来生存获益。
参考文献
1. Trigo J, Subbiah V, Besse B, Moreno V, López R, Sala MA, et al. Lurbinectedin as second-line treatment for patients with small-cell lung cancer: a single-arm, open-label, phase 2 basket trial. The Lancet Oncology. 2020;21(5):645-54.
2. Khurshid H, Ismaila N, Bian J, Dabney R, Das M, Ellis P, et al. Systemic Therapy for Small-Cell Lung Cancer: ASCO-Ontario Health (Cancer Care Ontario) Guideline. Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 2023;41(35):5448-72.
3. Cheng Y, Chen J, Zhang W, Xie C, Hu Q, Zhou N, et al. Benmelstobart, anlotinib and chemotherapy in extensive-stage small-cell lung cancer: a randomized phase 3 trial. Nature medicine. 2024.
4. Sen T, Takahashi N, Chakraborty S, Takebe N, Nassar AH, Karim NA, et al. Emerging advances in defining the molecular and therapeutic landscape of small-cell lung cancer. Nature reviews Clinical oncology. 2024;21(8):610-27.
5. Ahn MJ, Cho BC, Felip E, Korantzis I, Ohashi K, Majem M, et al. Tarlatamab for Patients with Previously Treated Small-Cell Lung Cancer. The New England journal of medicine. 2023;389(22):2063-75.
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理

