卒中的免疫机制和治疗
越来越多的证据提示,免疫系统在脑损伤过程中具有关键地位。免疫机制参与到缺血级联的每一个阶段;反过来,缺血性脑损伤也可以激活免疫系统或导致免疫抑制。
免疫激活与卒中风险
卒中前或卒中时的系统性炎症状态是卒中急性结局和长期预后的关键确定因素。很多传统的血管疾病危险因素,如动脉硬化、肥胖、糖尿病、高血压以及慢性感染本身就可以诱导慢性低水平炎症状态,并在感染等情况下启动急性炎症应答。
卒中的免疫激活
(1)脑源性抗原:长时间以来,脑部被认为是免疫豁免器官,血脑屏障破坏使中枢神经系统抗原接触并活化外周免疫系统。而新发现的脑部淋巴脉管系统,有可能直接解释脑源性抗原与周围免疫系统的相互作用。(2)细胞外释放分子:损伤相关分子模式是启动炎症介质上调的最主要信号。(3)免疫信号分子:细胞因子、趋化因子和黏附分子等免疫信号分子被激活。(4)自主神经系统信号:自主神经系统包括副交感神经系统和交感神经系统(SNS)。迷走神经是副交感神经系统的重要组成部分,迷走神经的免疫抑制效应被命名为脑-免疫机制、胆碱能抗炎通路或炎症反射。**迷走神经可能出现神经保护作用。SNS支配脾脏调节脾源性免疫细胞活化和它们浸润缺血脑组织,导致免疫应答激活。SNS也可造成脾脏萎缩,最终导致免疫抑制。
卒中后免疫应答
(1)先天性免疫应答:在急性脑损伤中提供最早期的应答,但下游通路的激活可能合并卒中后炎症并导致脑损伤。另一方面,通过参与卒中后修复,先天性免疫细胞可能也是保护性的。(2)适应性免疫应答:急性卒中后,适应性免疫系统被损伤部位释放的脑源性抗原活化。
卒中后免疫激活的消退和组织修复
卒中后免疫激活是自限性进程,最后消退并为损伤脑部的结构和功能重构作准备。炎症消退并不是促炎症因素耗竭后出现的消极过程,而是大量活性介质相互作用抑制炎症应答导致的。卒中后免疫抑制脑缺血后数小时内即可以出现全身免疫下调,即“卒中诱导的免疫抑制”.其机制尚未完全阐明,但可能涉及交感神经系统活化和伴随的甾类、儿茶酚胺类释放。
卒中后适应性免疫应答和免疫抑制的关系
卒中后的免疫激活或免疫抑制可能是一种对偶关系,炎症反应可以清除坏死组织,但过度的炎症会导致继发性组织损伤。反之,免疫抑制可能存在神经保护作用,但增加了感染的易感性。促进炎症和抗炎症免疫应答双方相互制约,可达到内环境动态平衡。
卒中的免疫学治疗
(1)卒中免疫学治疗的优势:首先,这些治疗有延长治疗时间窗的作用。其次,考虑到缺血再灌注也激活炎症反应,抑制炎症可作为溶栓或血管内取栓等再灌注治疗的适当补充。最后,炎症抑制在脑出血模型中有治疗作用,可以应用于出血性卒中尚不能排除的患者。(2)卒中免疫学治疗的存在问题:如卒中的动物模型不能完全重演人类疾病的病理。同时,限制缺血的炎症反应可以在急性期减轻组织损伤,却可能影响修复机制和恶化长期预后。更重要的是,我们目前对卒中病理生理的了解还很片面,因此应该充分考虑卒中免疫调节治疗的潜在风险,并小心平衡风险和获益之间的关系。
目前,由于免疫系统和中枢神经系统错综复杂的相互作用,尚未能精确地找到某一靶点作为卒中免疫学治疗的最佳途径,对卒中的免疫学治疗仍需保持谨慎的态度。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
热点图文
-
细数20年间卒中二级预防进展历程
让我们首先从抗血小板疗法来进行讨论。毫无疑问的是,阿司匹林对于卒中的二级预...[详细]
-
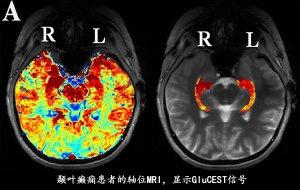
新型MRI成像技术可有效检出癫痫病灶
研究者正在尝试使用一种有力的影像学检查工具,对难以寻觅的癫痫病灶进行定位。...[详细]