帕金森病:起病年龄与大量微效基因联合作用相关
帕金森病(Parkinson disease,PD)是仅次于阿尔兹海默病的第二大神经退行性疾病。目前大多认为PD发病由遗传因素和环境共同引起。1997年发现了SNCA的第一个突变后,人们认识到,少数家族性早发PD可由单个罕见的高外显率基因突变引起。随后的全基因组关联研究(genome-wide association study,GWAS)发现了多于18个可能引起特发性PD的风险位点,但这些位点仅能解释3-5%的遗传性PD。
2009年Purcell等发明了多基因评分分析(Polygenic score **ysis)技术,证实了GWAS中无显著致病性的单核苷酸多态性(SNPs)叠加后可引起精神分裂症风险增加,且同样的风险SNPs也见于其他疾病队列。
2012年Keller等发现,当考虑微效基因位点后,GWAS数据中高达24%的遗传性PD病例可找到基因解释,因此推断PD可能是一个受多基因调控的遗传病。
近期,Valentina等在已有的四个GWAS数据库中,利用多基因评分分析技术证实了PD的易患性(liability)受大量微效基因的联合影响,早发PD并不仅仅由高外显率的孟德尔突变引起,多个较低风险的等位基因同时存在也可能导致早发PD。这项研究发表在今年的ANN NEUROL上。
考虑到起病年龄的临床记录可能不够准确,研究者选取起病年龄最小的5%病例(<40岁)和最年长的5%病例(>80岁)进行比较,发现起病年龄<40岁的患者,致病性SNPs评分明显高于起病年龄>80岁的患者。致病性SNPs评分>1.5分的患者,40岁之前起病的概率是80岁之后起病概率的4倍。
多基因评分分析技术的使用为证实PD相关微效SNPs的存在提供了可能,但PD的多基因信号传导和分子生物学机制仍未阐明。未来,随着基因通路分析(gene pathway **yses)技术的发展,相信PD的遗传学机制将逐步揭开神秘的面纱。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
- 相关阅读
- · 帕金森病的诊断鉴别
- · 帕金森遗传因素-临床执业医师复习精华
- · 左旋多巴药理|临床应用知识点
- · 帕金森病知识点及相关习题
- · 三分钟问卷,轻松检测路易体痴呆
热点图文
-
细数20年间卒中二级预防进展历程
让我们首先从抗血小板疗法来进行讨论。毫无疑问的是,阿司匹林对于卒中的二级预...[详细]
-
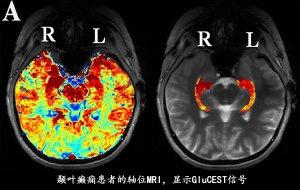
新型MRI成像技术可有效检出癫痫病灶
研究者正在尝试使用一种有力的影像学检查工具,对难以寻觅的癫痫病灶进行定位。...[详细]