HBV相关慢加急性肝衰竭抗病毒治疗的证据与特点
肝衰竭是多种因素导致肝功能严重障碍,出现已凝血障碍、黄疸、肝性脑病和腹水等为主要表现的临床症候群。根据组织学特点和疾病进展,我国2006年肝衰竭诊疗指南和2011年更新版肝衰竭诊疗指南,均把肝衰竭分为急性肝衰竭、亚急性肝衰竭、慢加急性肝衰竭(acute on chronic liver failure,ACLF)和慢性肝衰竭。目前我国肝衰竭的病因主要是HBV感染,临床以ACLF为主,疾病进展快,病死率高,因而受到广泛关注,其中抗病毒治疗是HBV-ACLF治疗的难点与热点。
HBV活动及反弹是ACLF重要促发因素
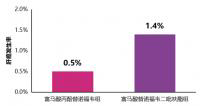
研究表明,我国HBV相关ACLF占到全部ACLF病例的70%——82%,在干扰素是禁忌证的情况下,与核苷(酸)类似物抗病毒治疗相关的因素列为可明确追寻的所有诱因之首。核苷(酸)类似物的中断、减量导致病毒反弹,或耐药引起的病毒学及生化学突破,是ACLF重要促发因素,占13.2%.其他促发或加重因素包括劳累(10.8%)、应用肝毒性药物(8.1%)、饮酒(3.5%)、腹腔感染(1.4%)。还有一大部分原因不明,推测有可能是其他病毒感染、肝内外血管病变、手术、出血等。
2009年亚太肝脏研究学会(APASL)首次以共识形式较系统阐述了ACLF定义,即在已存在或尚未发现的慢性肝病基础上,出现黄疸和(或)凝血功能障碍为表现的急性肝损害,发病4周内合并腹水和(或)肝性脑病,其中黄疸界定为血清胆红素≥5mg/dL,凝血功能障碍为INR≥1.5,或者凝血酶原活动度(PTA)<40%.同时,该共识也明确指出上述的慢性肝病基础包括各种原因引起的代偿期肝硬化、慢性肝炎、非酒精性脂肪性肝炎、胆汁淤积性肝病、代谢性肝病。此外共识还指出,急性打击事件包括感染因素,如嗜肝和非嗜肝病毒感染,乙型肝炎(显性或隐匿性)或丙型肝炎再活动,引起肝损害的其他感染性病原体,非感染性病因包括最近4周内饮酒,使用肝毒性药物、草药,自身免疫性肝炎或Wilson病发作,外科手术,未知肝毒性等病因,而对静脉曲张破裂出血没有达成共识。
欧洲肝脏研究学会(EASL)和美国肝病研究学会(AASLD)2011年发表的讨论意见亦认为ACLF多与急性打击事件有关,在已存在慢性肝病的基础上出现急性恶化,这与多系统器官衰竭而导致3个月死亡率增加相关,概念着重强调了器官衰竭,但基础肝病界定为肝硬化,即 “肝硬化亚组患者发生器官衰竭并随之需要住院治疗的综合征,可有或不能够被识别的促发因素病死率增加”.
虽然国内外对ACLF的认识和定义并不完全相同,但从该病的临床特点来看,ACLF是在慢性肝病的基础上出现急剧肝功能失代偿的临床症候群,但是与失代偿期肝硬化不同。ACLF在平时病情较为稳定,一旦在某些损伤因素的打击下,会出现肝功能急剧恶化并较快进展为器官功能衰竭。其中HBV**与反弹是HBV-ACLF公认的急性打击和促发因素,这也为HBV-ACLF的抗病毒治疗提供了例证。
HBV-ACLF发病机制尚不完全清楚,可能包括:①HBV感染:HBV-ACLF的始动和发生发展的重要因素,患者体内往往存在高水平的HBV DNA.②免疫损伤:HBV持续大量**是诱导强烈细胞免疫反应的重要因素,可能是ACLF发生和发展的主要机制之一。③HBV直接作用:细胞内过度表达的HBsAg可导致肝细胞损伤及功能衰竭;HBV的X蛋白也可引起肝脏损伤,在感染早期X蛋白使肝细胞对TNF-α等炎性介质更敏感而诱导细胞凋亡。④严重肝病导致的感染、出血、内毒素血症等。
HBV-ACLF抗病毒治疗的效果
**第302医院对2006年1月——2008年6月收治的348例HBV-ACLF患者作为研究对象,根据入组时病情分期及是否应用核苷(酸)类似物抗病毒治疗分为4组:早期未治疗组、早期治疗组、中期未治疗组和中期治疗组。统计每组患者4周生存率及病情好转率,并对348例患者2周时及184例患者 4周时的总胆红素(TBil)、ALT、PTA、终末期肝病模型(MELD)评分等进行组间比较分析。结果治疗2周时,早期未治疗组与早期治疗组、中期未治疗组与中期治疗组间,TBil、ALT、PTA 和MELD评分差异均无统计学意义(P值均>0.05)。治疗4周时,早期未治疗组与早期治疗组间,TBil、ALT、PTA和MELD评分差异均无统计学意义(P值均>0.05);中期未治疗组与中期治疗组间,PTA(分别为29.6%±9.6%和25.1%±9.1%)及MELD评分(分别为29.8±9.6和 22.1士9.1)差异有统计学意义(f值分别为-3.052和4.069,P值均<0.05)。治疗4周后,早期未治疗组与早期治疗组的HBV DNA转阴率分别为39.0%(16/41)和72.1%(44/61),4周生存率分别为53.4%(39/73)和75.0%(69/92),差异均有统计学意义(x2值分别为17.6l和8.38,P值均<0.01),中期未治疗组与中期治疗组的HBV DNA转阴率分别为42.3%(16/21)和80.4%(45/56),4周生存率分别为26.1%(24/92)和44.3%(47/106),差异均有统计学意义(x2值分别为10.98和7.13,P值均<0.01)。结论:应用核苷(酸)类似物抗病毒治疗可提高患者30 d生存率,是HBV感染所致ACLF内科有效治疗方法之一;HBV DNA转阴率、PTA及MELD评分可作为观察核苷(酸)类似物抗病毒近期疗效指标。
国内学者探讨了抗病毒治疗对低病毒载量的乙型肝炎相关ACLF患者转归的影响。352例乙型肝炎相关ACLF患者,其中低病毒载量组175例、高病毒载量组77例,各组分为护肝治疗(对照)组及抗病毒治疗组,比较两组患者临床特征、生存率及抗病毒治疗短期疗效差异。结果:观察24周,抗病毒治疗组的乙型肝炎相关ACLF患者总体生存率高于护肝治疗组(P=0.010),低病毒载量组中抗病毒治疗组的生存率高于护肝治疗组(P=0.001),高病毒载量组中抗病毒治疗组与护肝治疗组生存率差异无统计学意义(P=0.856),抗病毒治疗组中低病毒载量组与高病毒载量组的生存率差异无统计学意义(P=0.755)。由此得出结论:抗病毒治疗可提高低病毒**的乙型肝炎相关ACLF患者的生存率。
Yao-Li Cui等观察了HBV-ACLF应用核苷(酸)类似物治疗的安全性与效果。 研究者选择适合治疗的104例患者分为三组:A组口服ETV 0.5 mg,B组口服LAM 100 mg,C组不用核苷(酸)类似物。主要观察终点分别是3个月存活率和复发率,次要终点是血清HBV DNA水平、肝功能、MELD评分和不良反应。结果:3个月时三组存活率没有显著区别,但HBV DNA在治疗组明显要低。除了抗病毒组HBV DNA下降幅度明显高于未抗病毒组外,抗病毒组与非抗病毒组比较肝功能、MELD评分、肝功能恢复并未见到明显差异。但有意思的是,持续 1——3年的随访提示,抗病毒组复发率明显减少。由此作者得出结论:核苷(酸)类似物抗病毒治疗没有明显改善HBV-ACLF短期预后,但持续应用则有可能明显减少复发率从而提高远期存活率。
近期印度学者发表了类似研究的结果。在90例不同原因导致的ACLF中,27例因HBV重新活动引起,基线平均HBV DNA水平93 105 IU/mL.这些患者被连续纳入研究,并被随机分为替诺福韦酯组(14例)及安慰剂组(13例)。主要观察终点是3个月生存率。结果3个月时替诺福韦酯组生存概率明显高于安慰剂组(8/14 [57%] vs. 2/13 [15%]),P=0.03)。15例死亡病例死因是进展性肝功能衰竭导致多脏器衰竭。这些患者都没有条件进行肝移植手术。在替诺福韦酯组存活的病例中,Child-Pugh评分、MELD评分都有明显改善,血液HBV DNA 显著降低,而安慰剂组这些指标均无明显变化。2周时HBV DNA下降幅度超过2 log是***的生存预后因素。以此作者得出如下结论:替诺福韦酯能显著降低因HBV明显再活动引起的ACLF患者血液HBV DNA水平,改善Child-Pugh和MELD评分,降低病死率。2周时HBV DNA下降是可以采用的目标,它是患者生存与否的良好预后指标。
HBV-ACLF抗病毒治疗的特点
1. 早期:按照ACLF PIRO(predisposition, injury, response, organ)的概念图,若患者存在明确的急性打击因素,就需要尽快干预治疗,同时强化综合护理。既然HBV活跃**是HBV-ACLF的诱发因素,及早进行抗病毒治疗是需要的,过晚效果会大打折扣。多数研究也支持这一观点。
2. 强效:我国相关指南明确提出,对HBV DNA阳性的肝衰竭患者,无论其HBV DNA水平高低,建议立即进行核苷(酸)类似物抗病毒治疗。同时指出,拉米夫定、替比夫定、恩替卡韦更加强效快速,均可以应用(指南制定时,替诺福韦酯尚未在我国上市)。
3. 持续:考虑到ACLF患者病情严重及长期用药的问题,建议首选高效低耐药的核苷(酸)类似物,如恩替卡韦、替诺福韦酯等,以减少耐药发生维持长期治疗。
4. 综合:一个ACLF患者从控制肝脏炎症坏死-肝脏再生结构重建-功能恢复是一个漫长的过程,综合治疗必不可少,尤其要注意精神心理治疗、营养治疗和适当休息(PNR)。
总结
HBV-ACLF是进行抗病毒治疗的特殊人群。目前有较多的证据支持进行抗病毒治疗。早期、快速、强效、持续、综合是HBV-ACLF抗病毒治疗基本原则。树立PIRO+PNR理念有可能取得更好结果。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
- 相关阅读
- · 2016中西医医师考试辅导:新生儿黄疸的病因
- · 肝性脑病的概述、分型治疗
- · 新生儿黄疸延迟消退原因
- · 医生同志自我保护必读
- · 新生儿黄疸预防与护理方法
热点图文
-
AASLD2018研究进展丨慢乙肝患者治疗期间的肾脏安全管理
在新药取得成功之前,应用口服核苷(酸)类似物(NA)治疗慢性乙型肝炎(简称...[详细]
-
快讯丨TAF治疗4年的肝细胞癌发生率低于TDF
5月17日,在第十届全国疑难及重症肝病大会上,我国香港大学司徒伟基教授交流...[详细]