PSA阈值与MRI联合筛查策略的创新与临床影响
外科2024-09-18 10:35 浏览 :6887在前列腺癌筛查领域,传统的PSA筛查一直是主要的检测手段,但其局限性日益明显,尤其是在诊断敏感性和特异性方面的问题。哥德堡-2前列腺癌筛查研究通过创新性地结合PSA筛查和MRI技术,以期改进早期检测策略,优化临床治疗决策(图1)[1]。本文将详细探讨该研究的创新点,并分析其对临床诊疗的影响。
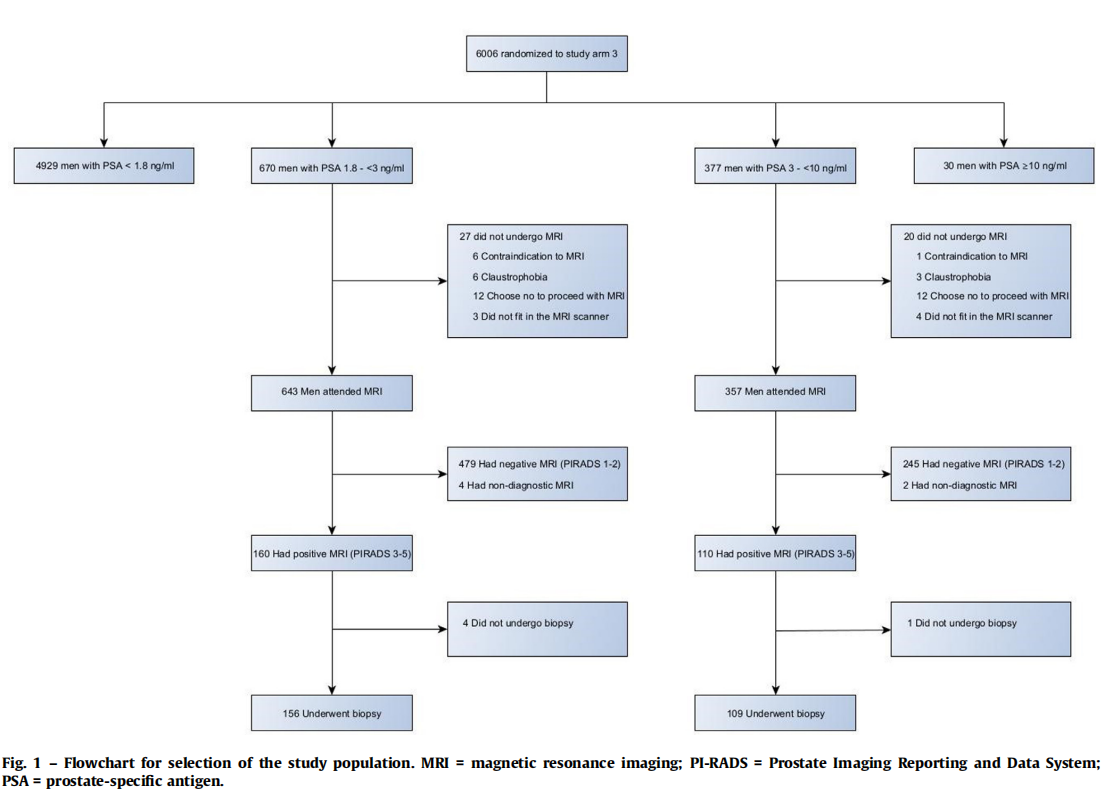
图1
一、研究的创新亮点
1. PSA阈值的调整
哥德堡-2研究最大的创新之一是在前列腺癌筛查中首次将PSA阈值从传统的3 ng/ml降低到1.8 ng/ml。这一改变的背后理念是:许多临床显著的前列腺癌可能存在于PSA值较低的男性中,通过降低阈值能够捕捉到这些潜在的高风险患者。传统筛查中,PSA值小于3 ng/ml的患者往往不会被视为高风险群体,而这一研究为早期发现此类患者提供了新的可能性。
2. MRI在低PSA人群中的应用
另一个重大创新是引入MRI作为筛查工具,特别是在PSA水平较低的男性中应用MRI。这一策略在筛查领域尚属前沿,旨在通过MRI的高精度影像,减少传统活检带来的过度诊断问题,同时提高临床显著前列腺癌的早期发现率。MRI的引入打破了单纯依赖PSA的局限性,使得诊断更加精准,并能在早期就锁定高风险病灶,避免错过临床显著癌症。
3.靶向活检的引入
哥德堡-2研究通过MRI筛查发现阳性病灶后,进一步进行靶向活检,而不是传统的系统性活检。靶向活检专注于MRI显像中出现的可疑区域,大大提高了癌症检测的准确性,减少了非必要的活检和随之而来的治疗过度问题。通过这种方式,研究不仅提高了癌症检出率,还减少了患者的创伤和并发症风险。
4. PI-RADS评分的优化使用
研究对PI-RADS评分的使用进行了深入分析,发现随着PI-RADS评分的升高,临床显著前列腺癌的风险也显著增加。这使得PI-RADS评分不仅仅作为MRI影像结果的指标,更成为评估癌症严重程度的重要工具。这种评分系统为临床医生提供了更好的决策依据,帮助他们在何时进行进一步的诊断和治疗上做出更为精准的判断。
二、临床诊疗的影响
1.早期发现临床显著癌症的机会增加
哥德堡-2研究显示,通过将PSA筛查阈值降低到1.8 ng/ml,并结合MRI筛查,能够在较低的PSA水平下发现更多临床显著的前列腺癌病例(表1)[1]。对于那些PSA在传统阈值以下的男性,这种筛查策略提供了早期发现癌症的机会,特别是Gleason评分较高的高风险患者。早期发现意味着这些患者能够更早接受治疗,进而提高治愈率并改善长期预后。
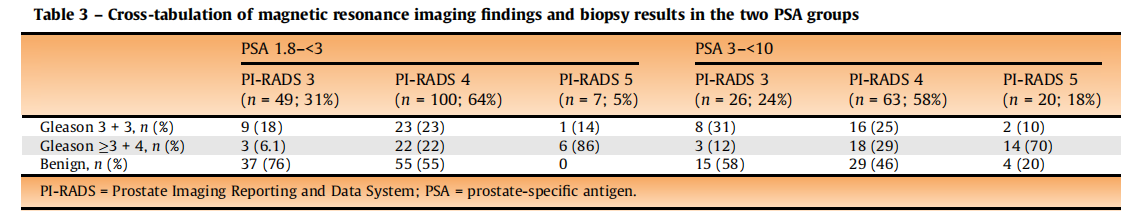
表1
2.减少过度诊断和治疗
在前列腺癌筛查中,过度诊断和过度治疗一直是困扰临床的难题。通过引入MRI和靶向活检,这项研究显著减少了临床不显著前列腺癌的诊断比例,从而降低了过度治疗的风险[1]。例如,许多Gleason 6分的前列腺癌患者可能并不需要立即治疗,而通过MRI筛查和靶向活检,可以更好地筛选出那些真正需要治疗的患者,减少不必要的干预和相关的并发症。
3.资源分配与成本效益的考量
尽管降低PSA筛查阈值并结合MRI显然能够提高临床显著癌症的检出率,但这一策略对医疗资源的需求也显著增加。研究指出,将PSA阈值降低至1.8 ng/ml,会使MRI的使用量增加2.6倍,这对医疗资源有限的系统来说是一个巨大的挑战[1]。如何在早期检测和资源利用之间取得平衡,将成为未来临床实践中的重要考量因素。因此,针对不同风险水平的患者群体进行分层筛查,或许是一个可行的方向。
4.个体化治疗决策的推进
该研究结果表明,通过MRI和PI-RADS评分系统,临床医生能够更加精准地评估患者的癌症风险,并据此做出个体化的治疗决策。这不仅能帮助患者避免不必要的手术或放疗,还能在恰当的时间点对高风险患者进行积极的干预(表2)[1]。对于那些PSA值较低但癌症风险较高的患者,个体化的筛查和治疗策略显得尤为重要。
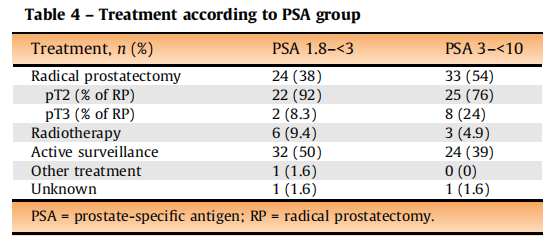
表2
5.临床指南的潜在修订
哥德堡-2研究的结果可能推动前列腺癌筛查指南的修订。目前,许多国家的筛查指南仍将PSA 3 ng/ml作为重要的分水岭,然而这一研究表明,降低PSA阈值并结合MRI筛查,能够发现更多的临床显著前列腺癌[1]。因此,未来的临床指南可能会更多地考虑个体化风险评估,并将MRI纳入常规筛查流程,尤其是在PSA较低的患者中。
三、结论
尽管哥德堡-2研究为前列腺癌筛查提供了许多新见解,但也留下了许多问题需要进一步探索。首先,未来研究需要更长时间的随访数据,以评估这种筛查策略对长期生存率和生活质量的影响。其次,在不同国家和地区推广这一策略时,必须考虑医疗资源的差异以及成本效益比。此外,未来可能还会引入新型的生物标志物或人工智能辅助的影像分析技术,以进一步提高筛查的精准性并优化筛查流程。
综上所述,哥德堡-2研究通过调整PSA阈值并结合MRI筛查,为前列腺癌的早期诊断提供了新的策略。它不仅提高了临床显著癌症的检出率,还减少了过度诊断和治疗的风险,推动了更加精准和个体化的临床治疗决策。这一创新性的筛查模式对未来前列腺癌的筛查和治疗具有重要的启示和影响。
参考文献:
[1] Möller F, Månsson M, Wallström J, Hellström M, Hugosson J, Arnsrud Godtman R. Prostate Cancers in the Prostate-specific Antigen Interval of 1.8-3 ng/ml: Results from the Göteborg-2 Prostate Cancer Screening Trial. Eur Urol. 2024;86(2):95-100. doi:10.1016/j.eururo.2024.01.017
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,如果您认为我们的转载侵犯了您的权益,请及时通过电话(400-626-9910)或邮箱(zlzs@120.net)通知我们,我们将第一时间处理,感谢。