病例汇报
患者,男,43岁,因“进食梗阻感进行性加重1个多月”于2020-01-07入院。患者1个多月前无明显诱因下出现进食梗阻感,无恶心呕吐,无呕血黑便等,症状逐渐加重,遂至当地医院就诊。2019-12-30查胃镜示:距门齿28-35cm可见半环隆起病变。胃镜病理示:(食管)鳞状细胞癌。PET/CT示:食管中下段管壁增厚伴FDG代谢增高,考虑食管癌(SUV=10.1)。降主动脉左侧旁有肿大淋巴结,FDG代谢增高,考虑转移(SUV=6.5);上腹部胃窦旁有肿大淋巴结,FDG代谢增高,考虑转移(SUV=7.5):纵隔内及两侧肺门有增大淋巴结,FDC代谢稍增高,考虑反应性增生。入院后,完善相关检查。2020-01-08胸部+上腹部增强CT示:食管中下段管壁不规则增厚,外膜面稍模糊,考虑食管癌,右上气管食管沟、纵隔、病灶周围、主动脉左后方多发淋巴结。双侧胸膜稍增厚,图1。2020-01-08病理会诊示:(食管)鳞状上皮重度异型增生、癌变。PD-L1CPS=15。心超、心电图、肺功能、颈部+锁骨上超声、喉镜等未见明显异常。 初步诊断:食管鳞癌,胸中下段,胃窦旁淋巴结转移,G1,cT3N2Ml,VB期(UCC第八版,2017)。
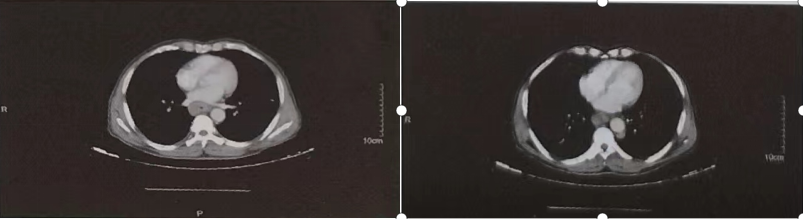
图1.胸部CT增强
第一次MDT讨论与治疗情况
胸外科:食管鳞癌诊断明确,制定治疗方案最重要的就是明确分期。该患者的疾病分期的要点在于腹部淋巴结。若该淋巴结为阳性,则分期为IVA期,无手术指征。肺部结节较小,难以一一穿刺活检;另外,主动脉左后方的淋巴结位置不属于食管癌的区域淋巴结。若该淋巴结为阳性,虽不影响分期,但会影响治疗方案的确定。该淋巴结不在食管癌的常规淋巴引流范围内,虽然考虑转移的可能性大,仍有可能是因其他因素导致良性淋巴结肿大。综上所述,可以先进行内科全身治疗,通过治疗后结合原发病灶、淋巴结的变化情况,对腹腔和主动脉后方淋巴结性质进行判断。
肿瘤内科:在全球范围内,每年食管癌可导致超过50万患者死亡,其中,食管鳞癌患者的占比为85%。对于转移性或晚期ESCC患者,既往标准的治疗为氟尿嘧啶类联合顺铂,但一线化疗给患者带来的总生存获益有限。2020年ESM0公布了KEYNOTE590Ⅲ期、随机双盲、安慰剂对照研究结果,评估帕博利珠单抗(P)联合化疗(C)与化疗作比较应用于晚期食管癌一线治疗中的效果。PD-L1CPS≥10的食管鳞癌中,P+C组的主要终点0S显著获益(13.9个月vs8.8个月;P<0.0001;HR=0.57);在食管鳞癌人群中,P+C组显著获益(中位0S:12.6个月vs9.8个月;P=0.0006;HR=0.72);在全人群中,P+C组的生存时间亦明显获益(中位0S:12.4个月vs9.8个月;P<0.0001;HR=0.73)。一线帕博利珠单抗联合化疗与安慰剂联合化疗相比,在OS、PFS和ORR的提升方面均有统计学意义和临床意义。2021年CSC0和NCCN指南都将帕博利珠单抗联合化疗纳入一线标准治疗。在化疗方案的选择上,国内的方案多选择紫杉类联合铂类,其有效率与氟尿嘧啶联合铂类相仿,临床应用上更为方便,也是CSC0指南的推荐之一。2021年更是有更多的免疫联合化疗用于晚期食管鳞癌的一线治疗数据。该患者有晚期食管鳞癌,CPS大于10,有条件可选择帕博利珠单抗联合化疗方案,化疗方案可选用氟尿嘧啶类/紫杉醇类联合铂类。
放疗科:患者有晚期食管中下段癌,PS的评分为0-1分,由于存在左后下纵隔淋巴结转移,分期为ⅣA期,手术无法做该处淋巴结的清扫,但可以为一个照射野所包含,建议行同步放化疗。另外,PD-L1CPS=15,根据KEYNOTE590等临床试验的报道结果,也可以进行免疫治疗联合化疗,后续根据免疫联合化疗效果进行根治性放疗。
治疗情况患者于2020-01-09、2020-02-01接受2周期化疗联合免疫治疗:白蛋白结合型紫杉醇200mg静滴d1、8,卡铂注射液570mg静滴dl,帕博利珠单抗200mg静滴dl,Q3W。2020-02-24复查胸部+上腹部增强CT,食管癌化疗后复查,对照2020-01-08CT:①食管下段病灶,较前缩小:纵隔多发转移性淋巴结,较前缩小。②胃窦旁转移性肿大淋巴结,较前明显缩小,见图2。疗效评价:PR。
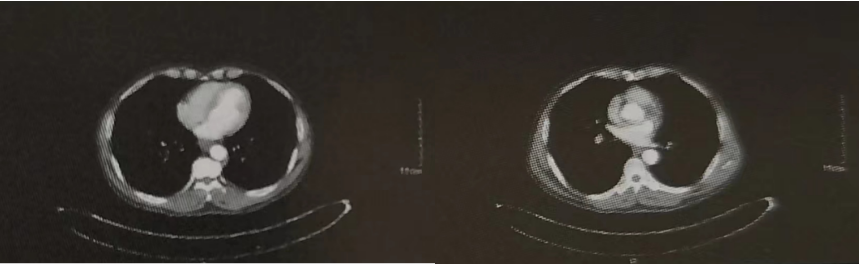
图2.胸部CT增强复查
第二次MDT讨论与治疗情况
胸外科:经过内科全身治疗后,肿瘤及纵隔淋巴结均缩小明显。腹腔淋巴结和胸主动脉后方淋巴结亦有缩小,提示该患者分期为ⅣA期,无手术指征。肿瘤内科:患者接受2周期免疫联合化疗后复查疗效为PR,后续继续原方案联合治疗最多6周期,后续进行免疫维持治疗。
放疗科:接受免疫联合化疗后食管病灶及纵隔转移淋巴结均缩小明显,根据KEYNOTE590等临床试验的结果可以继续行免疫联合化疗,也可以进行胃镜PET/CT等影像学评价,及时选择根治性放疗。若经过免疫联合化疗后食管及纵隔病灶均出现临床CR,则后续是否需要继续治疗暂无定论。根据CROSS等研究结果,即使出现了pCR的疗效,后续仍有相当比例的患者可能出现局部复发。因此,在此前提下,建议患者接受放疗以提高局部控制率。
治疗情况
患者于2020-02-25接受原方案第3周期化疗联合免疫治疗后,出现了Ⅱ度骨髓抑制,血小板偏低,予特比澳等治疗后好转。考虑患者的耐受性,决定行序贯放化疗。于2020-03-16至2020-04-21予食管病灶及纵隔、双锁骨上区淋巴引流区调强根治性放疗剂量为50.4Gy/28次。自2020-05-11至2020-06-22再按原方案行3周期化疗联合免疫治疗。患者于2020-06-29查胸部+上腹部增强CT,食管癌化疗后复查,对照前片:①食管中下段不均增厚;纵隔多发小淋巴结,均与前相仿。②原片中胃窦旁淋巴结,目前已不明显。疗效评价:PR。
第三次MDT讨论与治疗情况
放疗科:经过免疫治疗联合化疗序贯放疗后,影像学疗效评价为PR,后续该如何治疗自前仍无定论,是否需要免疫维持治疗仍然有待Ⅲ期随机对照临休试验的结果,由于该患者治疗前的PD-1CPS=15,其为相对高表达患者,理论上能够从免疫维持治疗中获益,因此,建议该患者进行帕博利珠单抗免疫治疗维持。
肿瘤内科:患者接受6周期免疫联合化疗后复查疗效为PR,根治性放疗耐受良好,后续进行免疫维持治疗。
治疗情况患者于2020-07-16开始行帕博利珠单抗200mg静滴Q3W治疗。2020-09-16查胸部+上腹部增强CT,食管癌化疗后复查,对照前片2020-06-29CT:①食管中下段稍增厚,较前相仿;纵隔多发小淋巴结,与前相仿。②考虑两肺纵隔旁放射性炎症,较前略明显,复查。2021-02-23查胸部+上腹部增强CT,食管癌化疗后复查,对照前片2020-11-27CT:①食管中下段稍增厚,较前相仿:纵隔多发小淋巴结,与前相仿。②考虑两肺纵隔旁放射性炎症,复查。患者于2021年4月开始自觉出现胸闷气急情况,并逐渐加重,遂再至我院就诊。2021-05-20查胸腹部增强CT,食管癌化疗后复查,对照前片2021-02-23CT:①食管中下段稍增厚,较前相仿;纵隔多发小淋巴结,与前相仿。②两肺多发斑片影,考虑炎症,范围较前明显增大,建议复查,见图3。血常规、C反应蛋白等感染指标未见明显异常。
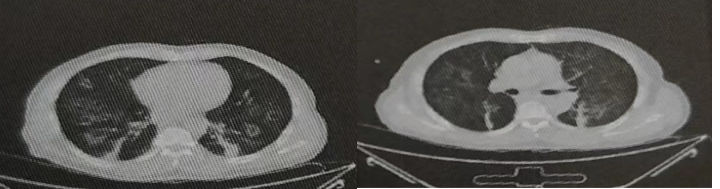
图3.胸部CT复查:双肺新出大片状磨玻璃影
第四次MDT讨论与治疗情况
影像科:食管癌化放疗后在免疫维持治疗中复查,对比放疗后的一系列CT片,双肺新出大片状磨玻璃影,以双肺内中带为主,边界模糊;结合患者的治疗史及临床症状、实验室检查,综合考虑免疫性肺炎的可能性大。
放疗科:患者放疗后出现呼吸困难,既往又使用过免疫药物,因此需要考虑免疫治疗相关肺炎合并放射性肺炎的可能。从影像学诊断看,间质性肺炎表现明显,治疗上暂停使用免疫治疗药物。其次,激素的使用也是必要的,常规使用1-2mgkg的强的松剂量,注意体温、痰培养等情况,若合并细菌感染,也需要使用广谱抗生素进行治疗。
肿瘤内科:患者在免疫治疗1年3个月后出现肺炎,结合影像和实验室检查考虑免疫相关性肺炎。根据免疫相关性肺炎不良事件的评级标准,该患者有呼吸道症状,CT提示当肺炎不超过50%肺实质的,可评为G2,治疗上应暂停免疫治疗,静滴甲基泼尼松龙1-2mg/kg,治疗48-72h后,症状有改善,激素在4-6周内按照每周5-10mg逐步减量。患者有明显的感染症状,暂不需加用抗生素治疗。
治疗情况患者于2021-05-21开始予甲强龙60mg静滴QD治疗。治疗后胸闷气急的表现较前好转。2021-05-31复查胸部CT,食管癌化疗后复查,对照前片2021-05-20CT:①食管中下段稍增厚,较前相仿;纵隔多发小淋巴结,与前相仿。②两肺多发斑片影,考虑炎症,局部较前吸收,见图4。遂予出院,甲强龙40mg口服QD,嘱每5天减量4mg。后患者已逐步减量并停用激素治疗。用药1个月后当地医院复查CT:肺炎已完全被吸收。后续患者未继续接受免疫治疗,定期复查。
总结
同步放化疗是局部晚期不可切除食管癌的标准治疗,由于以PD-1/PD-L1抑制剂为代表的免疫治疗药物的广泛应用,在同步放化疗的基础上联合兔疫抑制剂的研究目前正在开展之中,联合模式包括诱导免疫加同步放化疗、放化疗同步免疫药物以及同步放化疗后序贯免疫维持,究竟哪种模式更加合适,有待这些研究结果的公布。免疫治疗联合放疗需要警惕放射性肺炎的发生,免疫药物的加用有可能增加肺炎的发生概率,但是根据局部晚期非小细胞肺癌PACIFIC的研究结果,同步放化疗后序贯免疫维持不增加放射性肺炎的发生概率。一旦发生肺炎,暂停使用免疫治疗药物和放疗是首先需要考虑的,待肺炎治疗后恢复至I级后是否能够继续免疫治疗需要充分评价肺炎的风险和患者的获益程度。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,如果您认为我们的转载侵犯了您的权益,请及时通过电话(400-626-9910)或邮箱(zlzs@120.net)通知我们,我们将第一时间处理,感谢。





